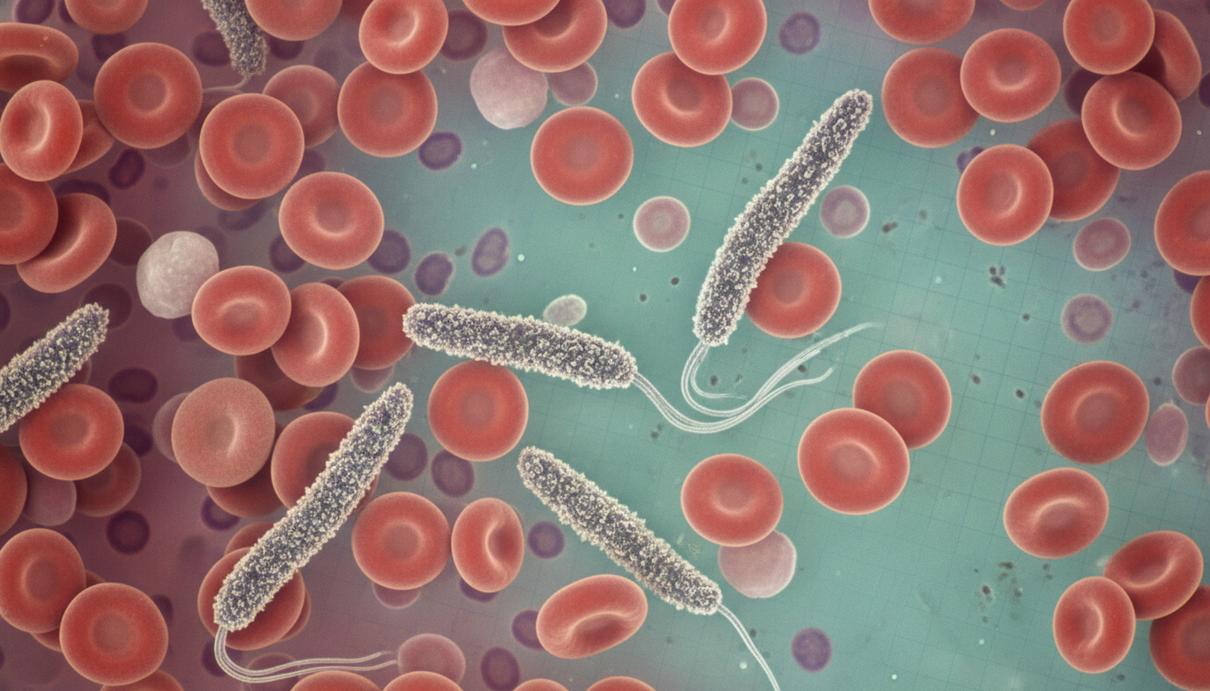
Группа ученых под руководством Йоркского университета идентифицировала белок, позволяющий африканской трипаносоме – возбудителю сонной болезни – эффективно скрываться от иммунной системы человека. Для выживания в кровотоке паразит использует защитную оболочку из вариантных поверхностных гликопротеинов. Результаты исследования, опубликованные в журнале Nature Microbiology, описывают ранее неизвестный механизм контроля этой молекулярной защиты.
Исследователи обнаружили, что ключевую роль в процессе играет белок ESB2. Он работает по принципу молекулярного измельчителя, который уничтожает определенные части генетических инструкций непосредственно в ходе их производства. Это позволяет паразиту оставаться незаметным для иммунитета, корректируя состав белков на поверхности клетки в режиме реального времени.
Открытие разрешает научную проблему, остававшуюся нерешенной более сорока лет. Биологи долгое время не могли объяснить асимметрию в экспрессии генов трипаносомы: гены, кодирующие защитную оболочку, и вспомогательные гены считываются одновременно, однако объем вырабатываемых ими белков существенно различается. Выяснилось, что паразит не ограничивает само считывание информации, а физически разрушает ненужные фрагменты матричной РНК сразу после их появления.
Белок ESB2 локализован в специализированном производственном центре паразита. В то время как генетический код преобразуется в инструкции для синтеза, белок подобно лезвию отсекает участки, относящиеся к вспомогательным функциям, не затрагивая при этом данные для формирования защитного слоя. Такая избирательность обеспечивает идеальное соответствие оболочки текущим условиям среды и минимизирует риск обнаружения антителами хозяина.
Сонная болезнь передается человеку при укусе мухи цеце и остается значимой проблемой для здравоохранения в странах Африки к югу от Сахары. При отсутствии терапии паразиты проникают в центральную нервную систему, что приводит к тяжелым нарушениям сна, когнитивным расстройствам и коме. Идентификация слабых мест в жизненном цикле трипаносомы, таких как механизм работы ESB2, создает основу для разработки новых методов лечения.
В международном проекте приняли участие специалисты из Великобритании, Португалии, Нидерландов, Германии, Сингапура и Бразилии. Работа проводилась при поддержке стипендии сэра Генри Дейла, фонда Wellcome Trust и Королевского общества. Исследователи отмечают, что выживание многих патогенных организмов может зависеть не столько от выпуска генетических команд, сколько от способности клетки уничтожать их непосредственно в источнике.